「参天製薬株式会社ってどんな会社?」
就職偏差値:Aランク
・緑内障/加齢黄斑変性/ドライアイ治療薬に強み
・一般用目薬は『サンテ』が主力
会社業績

(引用)SBI証券
会社概要
| 設立 | 1925年 |
|---|---|
| 資本金 | 85億2,500万円 (2021年3月31日現在) |
| 従業員 | 4,229名 (連結) (2021年3月31日現在) |
| 売上高 | 2,496億円(2021年3月期) |
事業区分
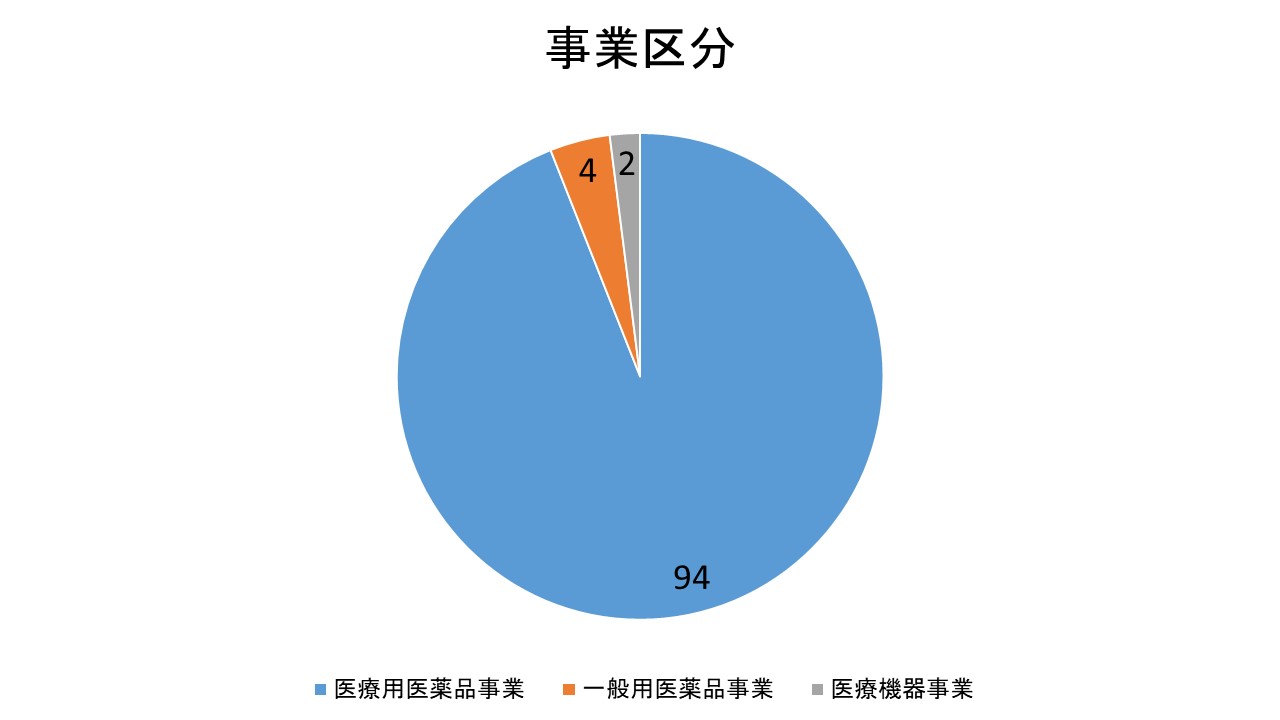
参天製薬株式会社は主に3つのセグメントから成り立っています。
・医薬品事業
・一般用医薬品事業
・医療機器事業
就活情報
平均年収:851万(平均年齢:43.9歳)
初任給
【MR職(医薬情報担当者)】
| 修士了 | (月給)340,200円 |
|---|---|
| 大学卒 | (月給)308,100円 |
【QC職(品質管理職)】
| 修士了 | (月給)340,200円 |
|---|---|
| 大学卒 | (月給)308,100円 |
【設備管理職】
| 修士卒 | (月給)340,200円 |
|---|---|
| 大学卒 | (月給)308,100円 |
| 高専卒 | (月給)256,800円 |
選考
エントリー → テストセンター(SPI) → 面接2回
☟適性検査の詳しい情報はコチラから!!☟
☟就活成功までの道のりはコチラから!!☟
事業詳細
医薬品事業
・医薬品の製造・販売
事業TOPIX
◎有価証券報告書(2021/4~2022/3)
日本
・前連結会計年度と比べ2.5%増加し、1,597億円となった。
中国
・円換算ベースで前連結会計年度と比べ16.6%増加し(為替影響を除いた成長率は+3.7%)、271億円となった。
・新製品であるジクアス点眼液及びタプロス点眼液の販売促進強化を行うとともに、主力製品であるクラビット点眼液及びヒアレイン点眼液は、集中購買による影響を受けつつも、引き続き私立病院や薬局など他のチャネルでの拡販に注力し、減少を抑制している。
アジア
・円換算ベースで前連結会計年度と比べ14.1%増加し(為替影響を除いた成長率は+7.9%)、192億円となった。
EMEA
・円換算ベースで前連結会計年度と比べ12.1%増加し(為替影響を除いた成長率は+6.1%)、413億円となった。
米州
・円換算ベースで23億円となった。
・米州の売上収益に含まれる、前連結会計年度に買収したEyevance Pharmaceuticals Holdings Inc.(米国)の売上収益は14億円。
一般用医薬品事業
・一般用医薬品の製造・販売
事業TOPIX
◎有価証券報告書(2021/4~2022/3)
・「サンテメディカルシリーズ」「サンテボーティエシリーズ」「ソフトサンティアシリーズ」などの高価格帯品に加え、スイッチOTC製品「ヒアレインS」、発売から2021年に30周年を迎えた「サンテFXシリーズ」に注力。
・前連結会計年度と比べ3.9%増加し、98億円となった。
医療機器事業
・医療機器の製造・販売
事業TOPIX
◎有価証券報告書(2021/4~2022/3)
・前連結会計年度と比べ28.4%増加し、52億円となった。
研究開発
研究開発TOPIX
緑内障・高眼圧症領域
・プロスタグランジンF₂α誘導体及びβ遮断剤の配合剤STN1011101(DE-111A、一般名:タフルプロスト/チモロールマレイン酸塩)は、中国で2019年1月から第Ⅲ相試験を実施。
・EP2受容体作動薬STN1011700(DE-117、一般名:オミデネパグ イソプロピル)は、米国で2021年11月に米国食品医薬品局(FDA)から審査完了通知を受領し、指摘事項への措置を講じたうえで再申請を行い、2022年6月に受理された。日本では2018年11月に発売。アジアでは、順次販売承認を申請しており、韓国で2021年2月に発売。
・FP/EP3受容体デュアル作動薬STN1012600(DE-126、一般名:sepetaprost)は、米国で2021年12月に追加の第Ⅱ相試験を終了した。日本では、後期第Ⅱ相試験を完了。欧州で2021年9月に第Ⅱ相試験(探索的試験)を開始。
・緑内障用デバイスSTN2000100(DE-128)は、日本で2022年2月に販売承認を取得した。欧州で2019年4月に発売。アジアでは、2020年3月以降順次販売承認を申請しており、2021年9月以降シンガポールなどで承認を取得。韓国で2021年4月に非承認通知を受理し、再申請を検討中。
・プロスタグランジンF₂α誘導体の乳化点眼剤STN1013001(DE-130A、一般名:ラタノプロスト)は、2022年3月に欧州及びアジアでの第Ⅲ相試験を終了。
・ROCK阻害剤STN1013900(AR-13324、一般名:netarsudil mesylate)は、日本で2020年11月から第Ⅲ相試験を実施。アジアで2022年3月に販売承認を申請した。
角結膜疾患(ドライアイを含む)領域
・春季カタルを対象とするSTN1007603(DE-076C、一般名:シクロスポリン)は、欧州、アジア、カナダなど既に承認・販売されている諸国に続き、中国では2022年4月に販売承認を取得。米国では2022年5月に発売。
・ドライアイを対象とするSTN1008903(DE-089C、一般名:ジクアホソルナトリウム)は、日本で2022年6月に製造販売承認を取得した。
・マイボーム腺機能不全を対象とするSTN1010905(一般名:シロリムス)は、日本で2021年10月に前期第Ⅱ相試験を開始した。
・アレルギー性結膜炎を対象とするSTN1011402(一般名:エピナスチン塩酸塩)は、日本で2022年2月に第Ⅲ相試験を開始した。
・フックス角膜内皮ジストロフィを対象としてアクチュアライズ株式会社と共同開発契約を締結しているSTN1010904*(一般名:シロリムス)は、第Ⅰ相試験を完了し、米国等での前期第Ⅱ相試験についてFDAへ治験届を提出した。(*開発コード(STN1010904)は、第Ⅱ相試験終了時に当社が独占的実施権を獲得した後に附番予定のコードです。)
網膜・ぶどう膜疾患領域
・ぶどう膜炎を対象とするSTN1010900(DE-109、一般名:シロリムス)は、事業性の再評価に基づき開発を中止。
新規疾患領域
・小児における近視を対象とするSTN1012700(DE-127、一般名:アトロピン硫酸塩)は、日本で2019年8月から第Ⅱ/Ⅲ相試験を実施。中国で2022年4月に第Ⅰ相試験を終了しました。アジアでは2020年4月に第Ⅱ相試験を終了した。
・小児における近視を対象とするSTN1012701(SYD-101、一般名:アトロピン硫酸塩)は、導入元であるSydnexis Inc.(米国)により欧州及び米国で第Ⅲ相試験が実施されている。欧州、中東及びアフリカ地域における独占ライセンス権を保有。
・近視を対象とするSTN1013400(化合物名:AFDX0250BS)は、日本で2021年9月に第Ⅰ相試験を終了。
・老視を対象とするSTN1013600(一般名:ウルソデオキシコール酸)は、日本で2022年4月に第Ⅰ相試験を終了。
まとめ
1.大手医薬品メーカー
2.抗がん剤/骨・関節領域に強み
3.ロシュ傘下で成長
参照・引用
公式HP:https://www.santen.com/ja/
就活生必見の記事
☟もっと企業研究をしたい方はコチラから!!☟